深圳先进院光遗传技术调控胶质细胞功能研究获进展
12月18日,国际学术期刊《自然-通讯》(Nature Communications) 发表了中国科学院深圳先进技术研究院王立平研究组的最新成果:用光遗传技术(Optogenetics,译为“光感基因神经调控技术”)调控胶质细胞对受损的多巴胺能神经元功能有重要的修复作用。该工作由杨帆、刘运辉、屠洁等研究人员完成。
传统观点认为胶质细胞对大脑功能只起辅助作用。近几年证据显示胶质细胞不仅参与一些特定脑认知功能,还对一些神经疾病发生发展起到重要作用。帕金森氏病是严重影响人类健康的重要脑疾病之一,其主要的病理改变是多巴胺神经元功能受损。通过调控大脑中数量最多的单一类的胶质细胞,来研究其对内源性多巴胺神经元及干细胞的作用,由于缺乏研究方法,始终难以实现。
胶质细胞作为大脑中数量最多的细胞,被证明可以通过分泌各类细胞因子和神经递质来影响神经元功能和干细胞的增殖分化。经典的研究方法针对不同种类的神经细胞功能调控缺乏高时空的精准和细胞特异性,致使无法精细理解大脑中细胞与细胞之间的相互作用机制。光遗传学技术为研究这样基本的科学问题提供了可能。
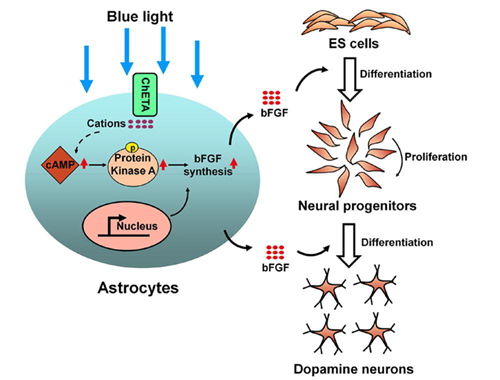
杨帆等将光遗传技术整合电生理和分子生物技术,首先将光感基因ChETA特异性的表达在培养的神经胶质细胞,发现蓝光刺激胶质细胞可以显著促进与其供培养的干细胞向神经元方向分化,而且分化成熟细胞具有典型的多巴胺能神经元的分子标记物和电生理学特征;他们还探索了其中的机制:光兴奋的胶质细胞可以激活蛋白激酶A和升高环磷酸腺苷浓度,促进胶质细胞释放成纤维生长因子(bFGF),从而起到对干细胞向多巴胺能神经元的分化的促进作用;他们还进一步证实体内活化的胶质细胞可以通过释放bFGF,有效促进移植干细胞向神经方向分化,有效改善帕金森氏病动物模型异常的行为;更重要的他们还首次证实了光特异性的调控内源性胶质细胞,可以明显提升受损黑质的bFGF水平,并显著促进受损脑组织的功能修复。黑质纹状体内的多巴胺神经元功能受损或缺失是导致帕金森氏病的主要原因,但是针对其内在的胶质细胞功能进行高时空精准的细胞调控,进而对受损的神经功能起到修复作用,国内外还没有报道。此项研究成果,有望为探索包括帕金森氏病在内的神经退行性疾病或其他精神疾病新的发生机制和治疗机理提供新的研究思路和理论支撑,也可为针对这些疾病研发新的药物或物理刺激治疗提供新的潜在治疗靶点。
近年来光遗传技术在神经科学领域获得了广泛的应用,Nature Methods杂志曾将此项技术评为2010年的年度技术。中科院深圳先进院王立平课题组经过几年发展,在国内搭建了功能较为完善的光遗传学研发、应用和资源共享平台,使其成为在神经环路水平上解析脑认知功能和复杂脑网络中神经细胞与细胞之间相互作用的重要方法。此实验室已经将相关技术方法向全国120多个脑科学实验室进行了辐射;为国内光遗传技术的应用和脑功能连接图谱方面整体研究水平的提升提供了技术上的支撑。今年年初,该课题组屠洁等采用光遗传学方法发现胶质细胞释放ATP对脑中风后神经功能修复有促进作用。这一系列工作的完成,建立并完善了一套动物在体光调控下生长因子检测方法,为细致研究大脑复杂神经环路中细胞与细胞之间的作用规律提供了新的研究手段。
该研究得到国家自然基金委员会重大研究计划(情感与记忆的神经环路基础)、中国科学院先导专项(脑功能连接图谱)、科技部、深圳市科技创新委等项目的资助。

