Adv Mater:南京大学沈群东教授光激活乏氧响应型共轭高分子纳米材
2016年3月7日,国际材料领域顶级期刊《Advanced Materials》在线发表了南京大学化学与化工学院沈群东教授领导的电活性高分子研究小组和北卡大学生物医学工程系顾臻教授领导的智能递药研究小组共同发表的一项研究成果,研究人员设计了一种新型的用于光动力治疗的制剂。整个体系基于一种光激活乏氧响应型共轭高分子纳米材料(CP-NI),能利用PDT产生的乏氧环境刺激抗肿瘤药物递送系统。在可见光的照射下,体系中的共轭高分子能诱导活性氧产生;与此同时,由该种高分子组成的纳米载体系统能够对诱导的乏氧环境进一步响应释放抗肿瘤药物。
南京大学博士生钱程根(北卡大学访问学生)、陈宇雷和北卡大学博士生俞计成为论文共同第一作者,沈群东教授和顾真教授为论文共同通讯作者。
光动力疗法(Photodynamic Therapy,PDT)是肿瘤治疗中最活跃的研究领域之一,它通过光照光敏剂引发活性氧生成而杀死肿瘤,是一种侵入性非常小的抗肿瘤手段。
该研究为刺激响应性药物递送系统提供一种新颖的设计策略:一种刺激元素能够激活肿瘤细胞内新的一系列刺激机关,从而加强协同治疗癌症的效果。在该项研究中,纳米载药体系通过尾静脉注射进入小鼠体内,经过血液循环富集到小鼠的肿瘤部位。此时对肿瘤处进行光照,在分子氧的参与下,CP-NI纳米体系的活性氧生成单元将被激活,开始消耗肿瘤处氧气以产生破坏性的活性氧;活性氧能氧化破坏各种生物大分子,使肿瘤细胞发生不可逆的损伤,促进体系溶酶体逃逸;同时肿瘤细胞内氧气的消耗将加剧乏氧环境,这时CP-NI中的第二个设计将被激活,2-硝基咪唑单元在乏氧的条件下被细胞内的生物体系还原成2-氨基咪唑,大大增强CP-NI在溶酶体中的溶解性,引起CP-NI纳米载药体系崩解,释放出运载的抗癌药物阿霉素(DOX)。释放的DOX和活性氧一同扮演灭杀伤癌细胞的角色,即光动力治疗和刺激响应性化疗协同作用。小鼠实验表明,该程序式递药技术能有效抑制肿瘤生长。光激活乏氧响应型共轭高分子纳米材料在生物医药材料中具有较好的应用前景。
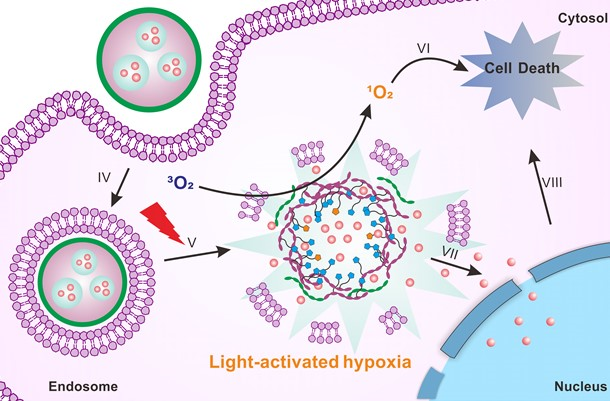
图:乏氧响应型共轭高分子纳米材料用作抗癌
原文链接:
Light-Activated Hypoxia-Responsive Nanocarriers for Enhanced anticancer Therapy
原文摘要:
A light-activated hypoxia-responsive conjugated polymer-based nanocarrier is developed for efficiently producing singlet oxygen (1O2) and inducing hypoxia to promote release of its cargoes in tumor cells, leading to enhanced antitumor efficacy. This dual-responsive nanocarrier provides an innovative design guideline for enhancing traditional photodynamic therapeutic efficacy integrated with a controlled drug-release modality.
作者:沈群东

