江南大学与Jens Nielsen实验室合作构建鸟氨酸高产酵母
鸟氨酸是氨基酸中间体,也是重要的医药原料和天然产物合成前体。2015年9月8号,Nature communication发表了江南大学和Jens Nielsen实验室构建鸟氨酸高产酵母的研究成果,工程酵母补料发酵可产鸟氨酸5.1 g/L。
作为食品添加剂和医药分子,谷氨酸棒杆菌无疑是最好的鸟氨酸(L-ornithine)细胞工厂,文献报道鸟氨酸的补料发酵浓度可达到40 g/L以上。作为天然产物(如莨菪烷生物碱,tropane alkaloids)合成前体,考虑到合成必需的P450氧化还原酶很难在细菌中表达,酿酒酵母则较谷氨酸棒杆菌更适合。而倘若工业化来生产这样的天然产物,直接补加较廉价的鸟氨酸似乎更合适。无论如何,这是首次报道构建高产氨基酸中间体的酿酒酵母,对其他类似产物细胞工厂的改造具有借鉴意义。
这里研究者应用模块化途径重构策略(modular pathway rewiring strategy,MPR)来提高葡萄糖到鸟氨酸产量。整个改造策略分为3个模块,1)鸟氨酸消耗模块;2)鸟氨酸合成模块;3)前体供应模块,即α-酮戊二酸合成模块。
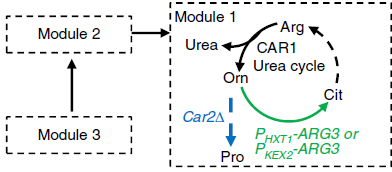
模块1
1)鸟氨酸消耗模块 改造该模块的目的是减少鸟氨酸向精氨酸、谷氨酸的转化,增加鸟氨酸的累积。下调鸟氨酸氨甲酰转移酶基因ARG3(弱化精氨酸合成),敲除鸟氨酸氨基转移酶基因CAR2(阻断鸟氨酸转化为L-谷氨酸-γ-半醛)获得工程菌M1c积累45 mg/L的鸟氨酸。

模块2
2)鸟氨酸合成模块 改造该模块目的是增加α-酮戊二酸向L-鸟氨酸的合成通量。考虑α-酮戊二酸在胞质中合成,而鸟氨酸在线立体中合成,因此这里有3种方法:
①不改变α-酮戊二酸或鸟氨酸的亚细胞定位。过表达精氨酸合成基因ARG5,6、ARG7、 ARG8,乙酰鸟氨酸合酶ARG2、线粒体膜上鸟氨酸转运体ORT1和精氨酸转运体AGC1,胞质中谷氨酸脱氢酶GDH1的工程菌M1cM2I可积累173 mg/L的鸟氨酸。
②将α-酮戊二酸合成转位到线立体,即在线粒体中引入谷氨酸脱氢酶,但谷氨酸在线粒体环境合成很少使该策略失败。
③在细胞质中重构鸟氨酸合成途径。通过在胞质中引入大肠杆菌来源的argAEC、argBEc和谷氨酸棒杆菌来源的argJCg、argCCg和 argDCg,同时过表达ORT1、AGC1和GDH1的工程菌M1cM2q可积累173 mg/L的鸟氨酸。说明在胞质中重引入完整的鸟氨酸合成途径比改造内源途径更适合于鸟氨酸的积累。
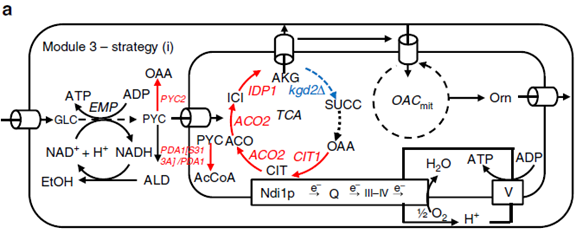
3)前体供应模块 目的是增加前体α-酮戊二酸供应,增强流向鸟氨酸合成的代谢流。这里研究者也采用了3种方法。
①过表达TCA循环中合成α-酮戊二酸相关的基因PDA1, PYC2, CIT1, ACO2 和 IDP1,工程菌M1cM2qM3a可积累245 mg/L的鸟氨酸,通过控制葡萄糖浓度的补料发酵可使鸟氨酸浓度达到5.1 g/L。
②过表达异源NADH氧化酶HaAOX1和内源的NADH脱氢酶NDI1可达到与直接增强TCA循环酶一样的效果,工程菌M1cM2qM3d可积累278 mg/L的鸟氨酸。
③通过过表达调控基因MTH1-△T降低糖转运体表达的工程菌M1cM2qM3e可积累778 mg/L的鸟氨酸,进一步过表达精氨酸合酶CAR1获得M1dM2qM3e可批次发酵产精氨酸1.041 mg/L。葡萄糖吸收速率降低导致菌株生长很差,弱化了代谢流流向乙醇合成(Crabtree effect),使这样的菌株并不适于工业化生产。
这是第一次构建酿酒酵母高产氨基酸中间体的细胞工厂,对其他类似中间体及其衍生化学品(天然产物)酿酒酵母细胞工厂的构建具有借鉴意义。
更多生物催化内容请关注微信公众服务号:生物催化剂设计与改造服务(STS-iDeep)
(发布:)


