生化与细胞所科研人员发现酵母KEOPS复合物参与细胞寿命调控
3月30日,《PLOS Genetics》在线发表了中科院上海生命科学研究院生物化学与细胞生物学研究所周金秋研究组揭示酵母KEOPS复合物调控细胞寿命的最新研究结果:“Inhibition of Telomere Recombination by Inactivation of KEOPS Subunit Cgi121 Promotes Cell Longevity”。该研究发现酵母KEOPS复合物亚基Cgi121通过参与端粒同源重组,增加基因组不稳定性,从而促进细胞衰老。
衰老是所有生物体共有的一个保守的生命现象。基因组的不稳定性被认为是造成衰老的一个重要原因。尽管真核生物的端粒(telomere)通常受到端粒酶(telomerase)的保护,但端粒与DNA双链断裂(DNA double strand break,DSB)的相似性使得它成为同源重组的易发位点。2009年,周金秋研究组的研究工作发现,端粒酶缺失后端粒重组的激活导致细胞寿命显著缩短。这一工作提示我们,端粒同源重组的发生能引发基因组不稳定性,从而加速细胞衰老。之后进行的遗传筛选鉴定到多个参与端粒重组的基因,这些基因被推测参与细胞寿命的调控,其中包括进化上高度保守的KEOPS复合物。
周金秋研究组的彭晶博士等以酿酒酵母为模式生物,阐述了KEOPS复合物亚基Cgi121调控细胞复制型寿命的分子机制。这一研究工作首先验证了端粒同源重组的激活加速细胞衰老,而抑制端粒重组后细胞寿命得以回复。Cgi121特异性地参与端粒同源重组。当CGI121基因缺失后,端粒同源重组效率降低,使得基因组更稳定,进而延长细胞寿命。值得注意的是,Cgi121并不影响另一重组高发区域——rDNA区域的同源重组,因此抑制端粒和rDNA区域的同源重组能叠加性地延长细胞寿命。进一步的机制研究表明,Cgi121可能是通过参与端粒末端单链DNA的产生来促进端粒重组,从而影响细胞寿命。这一工作揭示了同源重组与端粒酶竞争性地作用于端粒,从而影响细胞衰老的调控机制。
该研究得到了国家科技部和国家自然科学基金委的经费资助。(生化与细胞所)
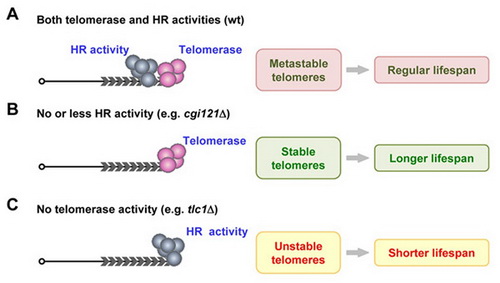
图:端粒同源重与端粒酶竞争性地作用于端粒,调控细胞寿命。
(A)野生型细胞中同源重组活性与端粒酶竞争,使得端粒处于亚稳定状态,导致普通长度的寿命。(B)当端粒重组水平降低时(如cgi121Δ突变体),端粒酶更好地保护端粒的稳定性,细胞寿命延长。(C)当端粒酶缺失后,端粒由于同源重组的作用而变得不稳定,细胞寿命缩短。
相关附件
