Nature Methods:新一代CRISPRs有望成为2015年重磅技术
当人们提到所谓的使能技术(enabling technologies),类似印刷机的发明,或者麻醉药的发现就会浮现在我们脑海中。而对于科学家来说,CRISPR-Cas9 系统就是这样一种系统。
这种细菌免疫系统能通过将病毒DNA中的短重复片段整合到细菌基因组中,来抵抗病毒。当细菌(或其后代)第二次感染病毒的时候,这些重复序列就能通过一种核酸酶靶向侵入的互补DNA,并摧毁它。
2013年几个研究组就利用了这一系统编辑真核生物基因,随后看到在不少应用中CRISPRs迅速崛起,多个不同物种都实现了基因组中基因删除和插入,激活或抑制基因转录。但是随着这一系统越来越受欢迎,关于其特异性和有效性的质疑也越来越多。
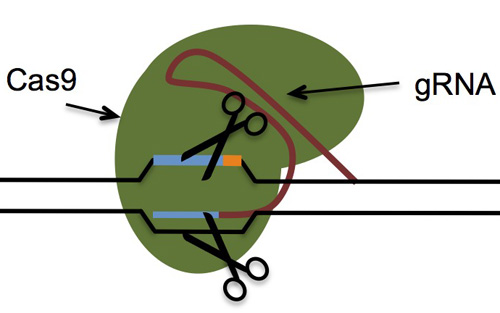
如何提高导向RNA(gRNA)的特异性是一大问题,这种RNA能将Cas9 核酸酶带领到基因组目标位置,Nature Biotechnology杂志建议切断gRNAs (Nature子刊:巧解基因编辑脱靶问题),减少脱靶问题,而且不影响靶标活性,而另外一个研究组则建议更长一些的gRNAs (Analysis of off-target effects of CRISPR/Cas-derived RNA-guided endonucleases and nickases)。
这明显是有些自相矛盾的建议,前者的研究人员指出只是简单截短了gRNA靶标区域的长度,结果发现在之前检测到的脱靶位点,脱靶突变都大幅减少,与全长gRNA相比,一些位点的突变频率甚至减少了5,000倍以上。重要的是在靶向它们的预定目标DNA时,这些缩短了的gRNA(称为tru-gRNA)与全长gRNA同样有效。而后者则发现选择合适的靶标序列,优化gRNA和Cas9,就能避免或者减少脱靶突变的出现。
另外一个问题是如何筛选脱靶,以及中对于研究的影响有多少。可以验证gRNAs错配候选位点的方法也许会错失一些关键的剪切位点,而且全基因组测序也不是非常有效,目前我们需要一种敏感且无偏差的方法,来标记Cas9 靶标位点,并令它们能在整个基因组中被识别出来。
其它的令这一系统特异性更强的方法还有,用配对替换切口酶(nickases)替换Cas9 核酸酶(前者每次只能切断DNA一条链),或者将 Cas9突变融合到Fok1 这种需要催化激活的核酸酶中去。此外,通过来自不同物种的Cas9也能增加靶向多个位点的灵活性,进一步改善 Cas9-gRNA 复合物的传递系统,也有助于增加效率。
尽管Cas9潜力无限,但是这还是一种细菌的蛋白,对于一些应用,尤其是临床上的应用来说,还需要寻找真核生物核酸酶进行替换。对于植物来说,一些Argonaute 核酸酶能通过小RNAs靶向DNA,这也是基因组编辑可以考虑的一个方向。

