生化与细胞所和计算生物学所合作最新研究成果:内含子来源环形RNA新分子及其转录调控功能机制
 9月27日,国际学术期刊《分子细胞》(Molecular Cell)发表了生物化学与细胞生物学研究所陈玲玲组与计算生物学所杨力组的最新合作研究论文,发现来源于基因内含子区域的环形RNA新分子,揭示其成环机制及在基因转录调控中的重要功能。
9月27日,国际学术期刊《分子细胞》(Molecular Cell)发表了生物化学与细胞生物学研究所陈玲玲组与计算生物学所杨力组的最新合作研究论文,发现来源于基因内含子区域的环形RNA新分子,揭示其成环机制及在基因转录调控中的重要功能。
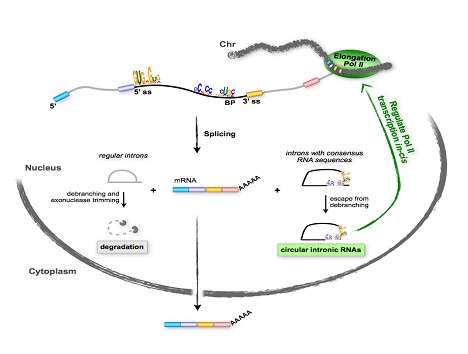
众所周知,人类基因组中存在大量被称为基因组“暗物质(dark matter)”的非编码序列,包括基因间非编码序列、内含子非编码序列等。基因间非编码序列转录产生线形长非编码RNA分子,具有5’帽子和3’尾巴结构;而内含子非编码序列转录生成的RNA在剪接后被核酸外切酶快速降解,多数没有生物学意义。陈玲玲研究组的最新研究成果发现了来源于内含子的环形非编码RNA新分子(circular intronic RNA, ciRNA),验证其在多种人源细胞内稳定存在,揭示其成环关键核酸序列及机制(即利用这些成环关键核酸序列诱导线形RNA成环)。
更为重要的是,研究还揭示了部分ciRNAs定位在其转录位点附近,并通过和RNA转录聚合酶Ⅱ复合物的互相作用,顺式调节其本位基因的表达水平。这项研究是该研究组在去年发表了内含子来源的sno-lncRNAs(Molecular Cell 2012年度最佳研究论文之一)后的又一重要发现。这些研究成果不仅发掘了蕴藏在人类基因组“暗物质”中的非编码RNA新分子,而且深入探索了这些新的长非编码RNA分子在基因表达调控中的重要功能作用。
最早的环形RNA分子在20世纪70年代于RNA病毒中发现。今年初,大规模测序证实了哺乳动物细胞内存在环形RNA,其通过“外显子反向剪接成环(back splice circularization)”形成,定位于细胞浆中,可以调控microRNA的功能。值得一提的是,陈玲玲研究组发现的ciRNAs与这些已知的细胞浆环形RNA在产生来源、加工生成、细胞内定位以及功能调控方面均有显著不同:ciRNAs来自于内含子序列,其生成依赖特定的成环关键核酸序列;成熟的ciRNAs定位在细胞核内并调控其本位基因的转录速度。因此,该项研究工作发现的内含子来源的环形RNA分子,在结构和概念上都是一类新型的长非编码RNA分子,进一步丰富了人们对真核细胞转录组表达调控多样性的认识。
该工作在当期Molecular Cell作为研究亮点(Issue Highlights)并获得专评(preview);该研究同时也获得了最近出版的Nature期刊的研究亮点专评(Research Highlights),题目为“环形RNA促进基因表达(RNA boosts genes on a loop)”。
生化与细胞所博士研究生张杨和计算生物学所博士研究生张晓鸥为本文的共同第一作者,该研究工作得到了国家基金委、科技部、中科院和上海市科委的经费支持。(生化与细胞所)

