表观遗传甲基转移酶SET8动态构象图景揭示其结构功能关系
5月13日,国际期刊eLife 在线发表了中国科学院上海药物研究所罗成课题组、美国纪念斯隆-凯特琳癌症中心Luo Minkui课题组与John D. Chodera课题组合作的研究成果“The dynamic conformational landscape of the protein methyltransferase SETD8”(DOI: 10.7554/eLife.45403)。该研究首次揭示了以SET8为代表的甲基化酶动态构象图景,为后续的SET8底物竞争和变构小分子抑制剂的设计提供了结构基础。同时,研究综合运用药物化学、结构生物学、化学生物学、分子模拟和机器学习等方法和技术,为多学科协同解决化学生物基础问题提供了范例。
甲基化转移酶是表观遗传领域的重要治疗靶标,现已有FDA批准的靶向甲基化酶的药物小分子用于临床,相关的基础研究和药物分子设计成为当今药物研究的重要领域。SETD8 (SETD8/Pr-SET7/KMT5A)是甲基化转移酶家族中的重要成员,是组蛋白赖氨酸H4K20的特异性单一甲基转移酶,参与转录调控、细胞周期调控、DNA损伤等多种生物学过程。相关研究表明,SET8在癌症的侵入、转移过程中发挥重要作用,其高表达还与儿科白血病及其存活率紧密相关。发展高活性、高选择性的小分子探针,通过靶向干预SET8以探索其结构功能关系不但可以推动表观遗传学基础生物学研究,同时可以促进相关的靶标成药性验证工作,还对药物发现与设计有着重要的科学意义。
该研究团队发现了SET8的高活性共价小分子抑制剂,并获得其复合物晶体。在总长达6毫秒的分子动力学模拟的基础上,运用机器学习的方法构建了马科夫状态模型(Markov state model),抽提出其SET-I domain介导的变构调节机制,并以此为依据进行了突变实验(K382P, I293G, and E292G)、ITC和停流动力学实验等验证。通过分析比较cBioPortal数据库中SET8的癌症突变数据,进一步印证了变构区域如何影响酶活的作用机制。
该研究主要由美国纪念斯隆-凯特琳癌症中心和中科院上海药物所的多个课题组合作完成,也得到了美国西奈山伊坎医学院、乔治亚大学、康奈尔大学和加拿大多伦多大学等合作支持。该研究还得到美国NIH、国家自然科学基金委、中科院、王宽诚教育基金会、新药创制重大专项和上海市科委等的资助。
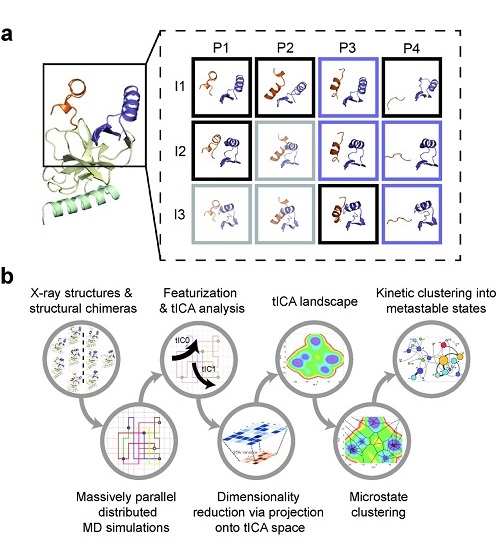
分子动力学模拟的构象图景的构建与马科夫状态模型

