武汉病毒所揭示病原细菌三型分泌系统主调控蛋白分泌机制
中科院武汉病毒研究所陈士云研究员领导的病原细菌学科组在耶尔森氏菌三型分泌系统主调控蛋白LcrQ分泌机制研究中取得重要进展,相关结果近期发表在国际微生物学刊物Molecular Microbiology。
三型分泌系统(Type III secretion system,T3SS)是革兰氏阴性病原细菌重要的毒力系统,研究其调控机制对控制病原细菌的感染具有重要意义。耶尔森氏菌的T3SS由一个毒力质粒编码,是研究T3SS调控及运转机制的重要模式菌株;其中LcrQ蛋白是T3SS主要的负反馈抑制因子,早在1995年就被鉴定参与耶尔森氏菌T3SS的负反馈抑制作用,全局性调控T3SS的表达和分泌。目前已知LcrQ在T3SS诱导条件下被分泌到细菌胞外激活T3SS,但尽管经历了将近20年的研究,LcrQ蛋白如何发挥负调控T3SS的功能以及LcrQ从细菌胞内被分泌到胞外的机制等研究一直没有进展。
该学科组博士生李云龙等通过构建毒力质粒上的基因过表达文库,筛选可以全局性调控T3SS的蛋白,结果发现分泌装置蛋白YscV在其中起到重要作用。通过构建yscV及yscV/lcrQ双缺失突变株等,发现YscV对T3SS的全局性调控作用依赖于LcrQ蛋白,并发现YscV不是通过影响LcrQ蛋白的表达而是直接控制LcrQ蛋白的分泌来实现其调控作用。进一步的细菌双杂交及Pull-down分析结果均表明,YscV的C末端493-511区域与LcrQ存在直接的相互作用,且该相互作用对LcrQ的分泌是必须的。基于以上结果,提出了依赖于YscV的LcrQ分泌介导的反馈抑制模型。这项研究首次揭示了分泌装置蛋白YscV在主调控蛋白LcrQ分泌过程中的功能,为T3SS负反馈调控机制的深入研究提供了新的思路,同时也为进一步系统阐释T3SS的调控机制提供了重要基础。
该研究得到了国家自然科学基金的资助。
文章链接
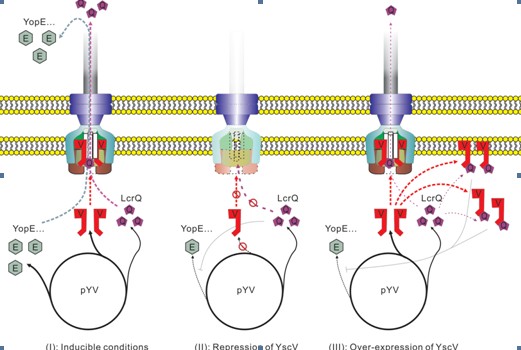
YscV依赖的LcrQ分泌及反馈抑制T3SS模型

