Science:美国科学家完成人类细胞全基因组范围内CRISPRs-Cas9敲除筛
包含麻省理工学院等机构的研究人员利用CRISPRs-Cas9技术完成人类细胞全基因组范围内敲除筛选。研究人员指出靶向同一基因的独立导向RNAs之间存在高度的一致性和高命中确认率,这对于Cas9基因组范围内筛选具有重要意义。相关文章发表于2013年12月12日的《science》杂志上。
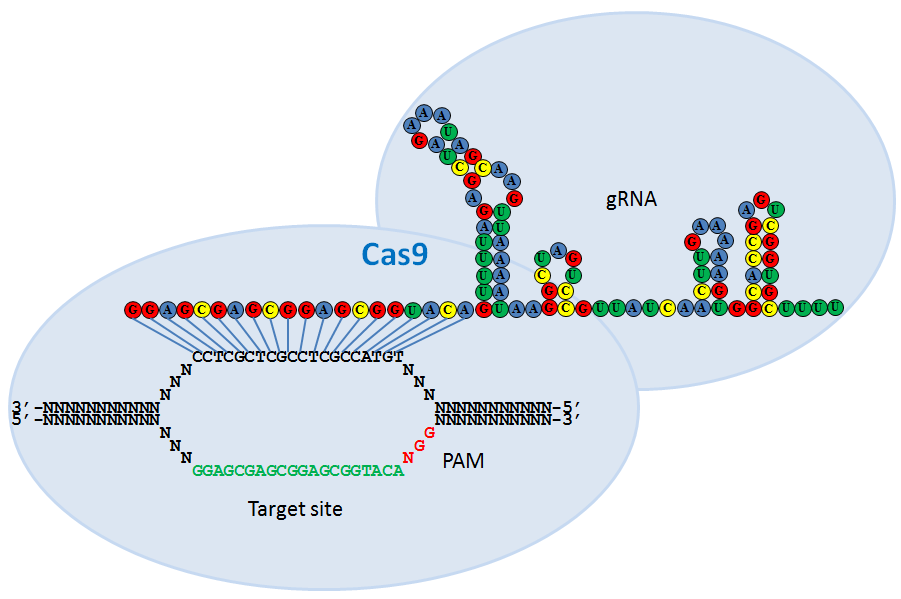
Science:美国科学家完成人类细胞全基因组范围内CRISPRs-Cas9敲除筛选
新宠儿——CRISPRs-Cas9技术
CRISPRs-Cas9技术成为了最近的新宠儿,这种基因组编辑技术更易于操作,也具有更强的扩展性。此前Zhang研究组曾利用细菌RNA,引导Cas9核酸酶在小鼠和人类基因组的特定基因位点上进行切割,完成了精确的目标链断裂。
Zhang表示,“CRISPR系统即使在从细菌细胞中取出酶和rna,然后再插入到哺乳动物细胞中之后,依然能如此有效的工作,这令人惊讶。”
CRISPRs-Cas9技术应用
在此基础上,研究人员发现靶向18,080个基因(64,751个独特靶向序列)的全基因组范围CRISPR - Cas9敲除(GeCKO)文库慢病毒传递,能在人类细胞中的正向和负向选择性进行筛选。
研究人员先利用GeCKO文库鉴定了对癌症和多能干细胞细胞活力必不可少的基因,其次他们还在一个黑素瘤模型中,筛选出了涉及药物维罗非尼(Vemurafenib)耐药性的基因。
从中研究人员筛选出了多个有效的基因,比如之前曾发现的NF1和MED12,以及未曾发现过的NF2,CUL3,TADA2B和TADA1 。
CRISPRs-Cas9技术发展
作者指出靶向同一基因的独立导向RNAs之间存在高度的一致性和高命中确认率,这对于Cas9基因组范围内筛选具有重要意义。
目前靶向基因组编辑技术已广泛用于基础研究和临床应用。CRISPR-CAS系统中的Cas9核酸酶能通过20nt导向序列靶向特异性基因组位点,允许某些与DNA靶标的错配,从而促进一些意外脱靶突变的形成。
Zhang研究组此前还揭示了一种增加基因组编特异性的新辑方法,即利用RNA导向的CRISPR-Cas9系统形成双切口,在未影响靶向切割效率的前提下,方便小鼠受精卵基因敲除研究。
作者简介
张锋(Feng Zhang,音译)是麻省理工学院脑与认知科学助理教授、McGovern 脑研究所和Broad研究所核心成员,今年七月,Feng Zhang荣获了美国生物医学大奖:瓦利基金青年研究家奖(Vallee Foundation Young Investigator Award),奖金25万美元。其研究组研究方向为设计新的分子工具来操控活体大脑。
原文摘要:
Genome-Scale CRISPR-Cas9 Knockout Screening in Human Cells
Ophir Shalem, Neville E. Sanjana, Ella Hartenian, Xi Shi, David A. Scott, Tarjei Mikkelson,Dirk Heckl, Benjamin L. Ebert, David E. Root, John G. Doench, Feng Zhang
The simplicity of programming the CRISPR-associated nuclease Cas9 to modify specific genomic loci suggests a new way to interrogate gene function on a genome-wide scale. We show that lentiviral delivery of a genome-scale CRISPR-Cas9 knockout (GeCKO) library targeting 18,080 genes with 64,751 unique guide sequences enables both negative and positive selection screening in human cells. First, we used the GeCKO library to identify genes essential for cell viability in cancer and pluripotent stem cells. Next, in a melanoma model, we screened for genes whose loss is involved in resistance to vemurafenib, a therapeutic that inhibits mutant protein kinase BRAF. Our highest-ranking candidates include previously validated genes NF1 andMED12 as well as novel hits NF2, CUL3, TADA2B, and TADA1. We observe a high level of consistency between independent guide RNAs targeting the same gene and a high rate of hit confirmation, demonstrating the promise of genome-scale screening with Cas9.

