两种植物提取物有助于抗癌
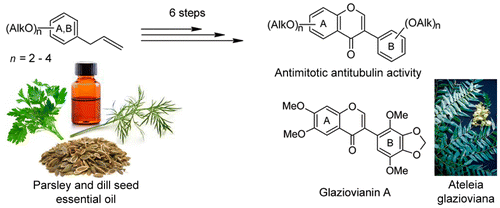
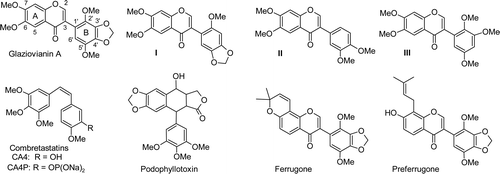
最近,俄罗斯莫斯科物理与技术研究院(MIPT)、N. D. Zelinsky有机化学研究所(RAS)、发育生物学研究所(RAS)以及细胞生物物理研究所(RAS)的一组科学家,提出了一种有效的方法来制备具有抗癌活性的新药物。这些药物的合成是基于从欧芹和莳萝种子中提取的化合物。这项研究结果发表在《Journal of Natural Products》杂志上。
MIPT教授Alexander Kiselev指出:“改善现有的治疗方法,并寻找创新的方法,是癌症治疗研究的重要组成部分。我们团队开发了一种简单的方法,利用来自大自然中切实可用的构建模块,生产glaziovianin A及其结构类似物。此外,我们使用确认的海胆胚胎试验,在体内评估了这些新药,筛选出了几种有前途的候选药物,能够有选择性地影响微管蛋白动力学。”没有癌细胞增长
目前,治疗癌症的主要方法是化疗。这种治疗使用抗有丝分裂剂,其通过破坏细胞分裂的过程(有丝分裂),而抑制癌细胞的生长。
癌细胞比正常细胞分裂的更加频繁,因此它们更容易受到抗有丝分裂剂的影响。例如,当细胞分裂受到刺激时,黑素瘤细胞的数量每3天增加一倍,而它们健康祖细胞——黑色素细胞的数量只增加了15%。
微管在有丝分裂中起着重要的作用。它们是由一种叫做微管蛋白的蛋白质组成的。抗有丝分裂剂可结合微管蛋白,并影响微管动力学,干扰细胞周期,从而导致细胞分裂停滞,以及随后的选择性死亡。这项研究集中在强效的抗有丝分裂剂glaziovianin A——从巴西树木Ateleia glazioviana Baill的叶子中提取出来。
这种药物已报道的合成方法是相当费力的,需要昂贵的前体(参与获得一个终产物所需的反应的物质)和催化剂(加速化学反应)。作者提出了一个新颖并更有效的六阶段glaziovianin A合成过程(正常过程有九个阶段),过程中的前体来自两种常见植物——欧芹和莳萝——的种子。
除了glaziovianin A之外,研究人员还合成了许多结构类似物,以帮助找到具有良好抗有丝分裂特性的类似物。研究人员通过两种独立的方法,使用海胆胚胎和人类癌症干细胞,检测了它们的抗肿瘤活性。
海胆和癌细胞
海胆的胚胎被用来模拟依赖于微管蛋白动力学而旺盛分裂的肿瘤细胞。科学家们向包含胚胎的水介质中添加了测试物质,并确定了分裂速度变化和分裂完全停止时的浓度。浓度越低,该物质的抗有丝分裂活性就越大。就像研究人员以前确定的那样,当细胞分裂被一种药物的特效抗微管蛋白活性而中断时,海胆的胚胎开始轴向旋转。使用普通光学显微镜,就可以很容易、很方便地观察到这种效应。
使用胚胎,科学家们能够一次性地确定一种抗癌分子所必需的几个重要参数。包括特定的抗有丝分裂作用、溶解度、总体毒性和生物膜通透性。
为了进一步证实活效分子的抗肿瘤作用,他们研究了各种人类癌症细胞,例如肺癌、黑色素瘤、前列腺癌、乳腺癌、结肠癌和卵巢癌。实验表明,测试物质有效地限制了黑色素瘤细胞的生长,对于作为对照的健康血细胞则是无毒的。在这两个试验系统中,详细的结构-活性关系研究指出,glasiovianin A是最活跃的抗有丝分裂剂。下一步的计划包括,对化合物进行优化,以改善其代谢稳定性和溶解性,以及在小鼠身上开展人类异种移植研究,以证实它们的抗肿瘤活性和临床发展潜力。
2015年8月,来自美国宾夕法尼亚州立大学的一组研究人员报道称,在紫土豆中发现的化合物,可能有助于杀死结肠癌干细胞,并限制癌症的扩散。这项研究结果发表在国际期刊《Journal of Nutritional Biochemistry》。相关阅读:土豆提取物杀死癌症干细胞。
2015年10月,来自美国埃默里大学Winship癌症研究所、芝加哥大学、UT西南医学中心、北京大学和复旦大学等处的科学家发现,在地衣和大黄中提取的一种橙色色素——称为蜈蚣苔素(parietin),可能有潜力作为一种抗癌药。相关研究结果发表在《Nature Cell Biology》。相关阅读:中美学者:一种天然提取物可抗癌。
最近在《Molecular Oncology》发表的一篇文章中,美国勘萨斯大学癌症中心的徐博士和Neufeld似乎已经发现了一种潜在的药物,是一种棉籽提取物——棉酚,棉花植物中的一种天然成分,目前正处于前列腺癌临床试验的早期阶段。(来源:生物通 王英)
Efficient Synthesis of Glaziovianin A Isoflavone Series from Dill and Parsley Extracts and Their in Vitro/in Vivo Antimitotic Activity
Abstract A concise six-step protocol for the synthesis of isoflavone glaziovianin A (GVA) and its alkoxyphenyl derivatives 9 starting with readily available plant metabolites from dill and parsley seeds was developed. The reaction sequence involved an efficient conversion of the key intermediate epoxides 7 into the respective β-ketoaldehydes 8 followed by their Cu(I)-mediated cyclization into the target series 9. The biological activity of GVA and its derivatives was evaluated using a panel of seven human cancer cell lines and an in vivo sea urchin embryo assay. Both screening platforms confirmed the antimitotic effect of the parent GVA (9cg) and its alkoxy derivatives. Structure–activity relationship studies suggested that compounds 9cd and 9cf substituted with trimethoxy- and dillapiol-derived B-rings, respectively, were less active than the parent 9cg. Of the evaluated human cancer cell lines, the A375 melanoma cell line was the most sensitive to the tested molecules. Notably, the target compounds were not cytotoxic against human peripheral blood mononuclear cells up to 10 μM concentration. Phenotypic readouts from the sea urchin assay unequivocally suggest a direct microtubule-destabilizing effect of isoflavones 9cg, 9cd, and 9cf.
原文链接:http://pubs.acs.org/doi/pdf/10.1021/acs.jnatprod.6b00173

