Cell:科学家揭示L1跳跃基因与宿主控制机制之间存在着军备竞赛
约翰霍普金斯大学基础生物医学科学研究所博士后戴立新领导的研究组,在新研究发现,驱使迁移至人类基因组新区域的跳跃基因,与致力于限制这样的不稳定DNA片段所带来的风险的细胞之间存在着军备竞赛。相关文章发表于2013年11月21日的《Cell》杂志上。
跳跃基因基本了解
跳跃基因,正式应称作为转座子或转座元件,这类dna片段携带着一些蛋白质蓝图,生成的蛋白质可帮助这种DNA片段复制或将它从基因组的一个位置剪切出来,再插入到一个新位点。
人类基因组散落着一些远古跳跃基因的残留物,但我们的细胞已经进化了一些途径来调控它们,限制这样的侵入。大多数的跳跃基因已发生突变,不再能够移动,但这些“锈迹斑斑的船体”仍然一代一代传递下来。
L1跳跃基因是一个例外,它是如此的成功,其拷贝构成了大约20%的人类DNA。尽管其中的许多拷贝现在已经突变及处于静止状态,但另一些仍然活跃,遗传学家对它们非常的感兴趣。
该研究的领导者、约翰霍普金斯大学基础生物医学科学研究所博士后戴立新(Lixin Dai ,音译)说:“人类细胞已经进化出了一些途径来限制跳跃基因的活性,因为它们越是频繁地移动,越有可能破坏重要的基因,造成严重的损害。”
L1跳跃基因研究
为了更多地了解细胞控制L1的机制,以及跳跃基因利用了哪些诡计来逃避这些防御,戴立新和Jef Boeke实验室的其他研究人员,首先诱导实验室培养的人类细胞生成了大量L1 蓝图编码的蛋白质。正如预期的那样,两种L1蛋白结合一些人类蛋白质和RNA遗传物质形成了所谓的核糖核蛋白颗粒复合物——L1利用了它来进行“跳跃”。
为了弄清楚哪些人类蛋白与核糖核蛋白相互作用,因此有可能在抑制它的活性或帮助它移动中起作用。Boeke研究小组与洛克菲勒大学的研究人员展开了合作。洛克菲勒大学的研究人员曾开发了一种技术,用液氮快速冷冻酵母,然后用钢球碾碎它,再用微小的磁性粒子非常快速地抽提出核糖核蛋白。“这是一种极好的维持相互作用的方法,”戴立新说。
将这一强大的技术应用于人类细胞,研究小组发现有37个蛋白似乎与核糖核蛋白互作,他们挑选出了两个进行进一步的分析。其中一个叫做UPF1的蛋白,已知在质量控制中起作用;它负责监控并破坏出错的rna转录物。戴立新说,在这种情况下UPF1结合到了L1核糖核蛋白上。当研究人员让UPF1基因丧失功能时,发现细胞生成了更多的L1 RNA和蛋白质。但他们仍然没有弄清楚UPF1确切是如何与核糖核蛋白进行相互作用的。
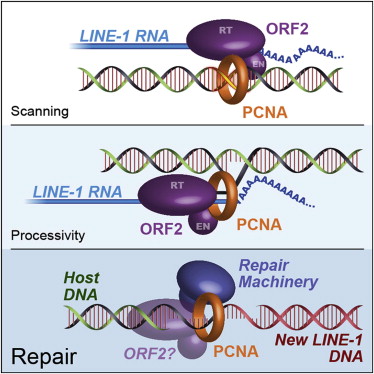
另外一个人类蛋白PCNA,可细胞发生分裂之前帮助拷贝DNA链。研究人员发现PCNA与核糖核蛋白其中的一个L1蛋白的一个重要片段发生了相互作用;当他们尝试去改变这一片段时,L1不再能够跳跃。相比UPF1起抑制L1活性的作用,PCNA似乎加入进来帮助了跳跃基因,其或许在L1剪切自身进入到一个新位点时帮助修复了人类DNA中留下的缺口。
戴立新指出,没有该研究中采用的两种开拓性的方法:大量培育人类细胞并诱导它们生成核糖核蛋白,以及采用快速冷冻技术在人类细胞中研究相互作用,不可能获得这些研究发现。他预计,这些方法将大大增进生物学家们对于L1的理解,这一跳跃基因在人类基因组的进化中起着重要的作用,其活性与某些癌症有关。
“我们的研究揭示了跳跃基因是如何试图变得灵活逃避宿主控制机制,以及宿主是如何将其活性限制到最小程度的机制。我们期待更多地了解这一军备竞赛。”
原文摘要:
Affinity Proteomics Reveals Human Host Factors Implicated in Discrete Stages of LINE-1 Retrotransposition
Martin S. Taylor,John LaCava,Paolo Mita,Kelly R. Molloy,Cheng Ran Lisa Huang,Donghui Li,Emily M. Adney,Hua Jiang,Kathleen H. Burns,Brian T. Chait,Michael P. Rout,Jef D. Boeke,Lixin Dai
LINE-1s are active human DNA parasites that are agents of genome dynamics in evolution and disease. These streamlined elements require host factors to complete their life cycles, whereas hosts have developed mechanisms to combat retrotransposition’s mutagenic effects. As such, endogenous L1 expression levels are extremely low, creating a roadblock for detailed interactomic analyses. Here, we describe a system to express and purify highly active L1 RNP complexes from human suspension cell culture and characterize the copurified proteome, identifying 37 high-confidence candidate interactors. These data sets include known interactors PABPC1 and MOV10 and, with in-cell imaging studies, suggest existence of at least three types of compositionally and functionally distinct L1 RNPs. Among the findings, UPF1, a key nonsense-mediated decay factor, and PCNA, the polymerase-delta-associated sliding DNA clamp, were identified and validated. PCNA interacts with ORF2p via a PIP box motif; mechanistic studies suggest that this occurs during or immediately after target-primed reverse transcription.

