Cell子刊:中国科学家对两种重要细胞重编程技术进行比较获新发
北京生命科学研究所的研究人员对两种重要的细胞重编程技术进行比较,结果表明SCNT介导的重编程相比于基于iPSC的重编程技术,更大程度上减轻了端粒功能障碍和线粒体缺陷。这一研究发现为了解这一差异的基本机制将可能有助于优化重编程策略。相关文章发表于2013年11月21日的《Cell stem cell》杂志上。
Cell子刊:中国科学家对两种重要细胞重编程技术进行比较获新发现
北京生命科学研究所的高绍荣(Shaorong Gao)研究员和杭州师范大学衰老研究所的鞠振宇(Zhenyu Ju)研究员是这篇论文的共同通讯作者。
体细胞重编程是指将分化末端的体细胞重编程转变回多潜能状态,再通过定向分化可获得特定类型的细胞,这一技术在再生医学领域具有十分重要的应用前景。当前,SCNT技术和iPS技术是进行体细胞重编程的两项重要研究方法。
SCNT技术研究
所谓SCNT是指将一个动物细胞和细胞核移植至去核的卵母细胞中,产生与供细胞核动物的遗传成份一样的动物的技术。1996年7月,英国科学家伊恩•维尔穆特博士利用SCNT成功克隆出了一头小羊,并取名多利(Dolly)。随后,研究人员利用该技术在牛、山羊、小鼠等物种上均获得了成功。
这些成功案例激发了研究人员对“治疗性克隆(Therapeutic Cloning)”的展望,也就是说如果能通过这种方式获得某人的胚胎干细胞,也就可以制造出该机体的各类细胞,这样就可以方便研究人员构建疾病模型进而研究治疗相关疾病的方法。不过直至今天SCNT技术实际进展仍受到诸多限制。
ips技术发现及展望
2006年京都大学教授山中伸弥开发出了一种能将体细胞重编程为多潜能干细胞样细胞的iPS技术,这种方法制备简单,只需要将几个关键的与细胞多潜能状态有关的转录因子转入体细胞并使其过表达即可。
由于iPS细胞具有与胚胎干细胞类似的功能,又绕开了胚胎干细胞研究面临的伦理和法律等诸多障碍,这一研究领域近年来以极其迅猛的速度发展。然而,直到现在人们对于两种技术及其所生成的多能干细胞还没有进行过详细的比较分析。
两种技术比较
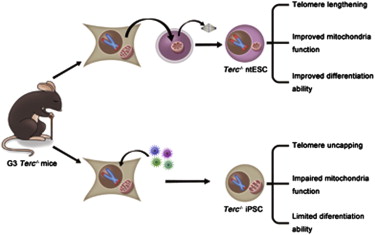
研究人员利用显示端粒功能障碍和早衰的端粒酶敲除(Terc-/-)小鼠,检测了两种重编程方法恢复端粒活力的能力。他们发现相比于Terc-/- iPSCs,来自Terc-/- SCNT胚胎的胚胎干细胞(Terc-/- ntESCs)具有更强的分化潜能和自我更新能力。
值得注意的是,SCNT克隆胚胎中端粒显著延长,Terc-/- ntESCs中端粒戴帽功能增强。此外,研究人员发现Terc/ iPSCs和它们的分化衍生物中线粒体功能严重受损,而在Terc-/- ntESCs中线粒体功能则得到显著改善。
这些结果表明SCNT介导的重编程相比于基于iPSC的重编程技术,更大程度上减轻了端粒功能障碍和线粒体缺陷。研究人员认为了解这一差异的基本机制将可能有助于优化重编程策略。
作者简介:
高绍荣博士主要从事哺乳动物体细胞克隆胚胎发育过程中再编程的分子机理研究, 其曾首次利用iPS细胞克隆出活体实验鼠,证实iPS细胞与胚胎干细胞一样具有全能性,这一成果入选了美国《时代周刊》评选的2009年全球十大生物医学进展,并为中国干细胞研究赢得了话语权。鞠振宇博士的主要研究方向是成体干细胞和衰老生物学的研究。
原文摘要:
Enhanced Telomere Rejuvenation in Pluripotent Cells Reprogrammed via Nuclear Transfer Relative to Induced Pluripotent Stem Cells
Rongrong Le,Zhaohui Kou,Yonghua Jiang,Ming Li,Bo Huang,Wenqiang Liu,Hui Li,Xiaochen Kou,Wanzhong He,Karl Lenhard Rudolph,Zhenyu Ju,Shaorong Gao
Although somatic cell nuclear transfer (SCNT) and induction of pluripotency (to form iPSCs) are both recognized reprogramming methods, there has been relatively little comparative analysis of the resulting pluripotent cells. Here, we examine the capacity of these two reprogramming approaches to rejuvenate telomeres using late-generation telomerase-deficient (Terc−/−) mice that exhibit telomere dysfunction and premature aging. We found that embryonic stem cells established from Terc−/− SCNT embryos (Terc−/− ntESCs) have greater differentiation potential and self-renewal capacity than Terc−/− iPSCs. Remarkably, SCNT results in extensive telomere lengthening in cloned embryos and improved telomere capping function in the established Terc−/− ntESCs. In addition, mitochondrial function is severely impaired in Terc−/− iPSCs and their differentiated derivatives but significantly improved in Terc−/− ntESCs. Thus, our results suggest that SCNT-mediated reprogramming mitigates telomere dysfunction and mitochondrial defects to a greater extent than iPSC-based reprogramming. Understanding the basis of this differential could help optimize reprogramming strategies.

